Título
Autor
Lugar de Realización
Correspondencia
Texto
HIDROCEFALIA EXTERNA DEL ADULTO. MANEJO TERAPÉUTICO Y DIAGNÓSTICO DIFERENCIAL CON HEMATOMA SUBDURAL CRÓNICO E HIGROMA SUBDURAL
Presentación de un caso y revisión de la literatura
Matías Rojas, Guillermo Vergara, Ernesto Castellaní, César Sereno, Andrés Cervio, Jorge Salvat
Departamento de Neurocirugia. Instituto de Investigaciones Neurológicas Raul Carrea. FLENI
RESUMEN
Objetivo. Presentar un caso de hidrocefalia externa en un adulto.
Presentación. Paciente de 73 años con trastornos en la marcha y paresia braquial derecha de tres semanas de evolución secundarios a hematoma subdural (HSD) frontotemporoparietal izquierdo.
Intervención. Tras doble evacuación y craniectomía descompresiva por resangrado en postoperatorio inmediato. evolucionó con sensoriofluctuante y confuso, evidenciando en tomografías computadas (TAC) controles colecciones liquidas bilaterales extraaxiales con ventrículos, surcos y cisternas conservados, "signo de venas corticales" a través de cada colección con herniación de ésta a través de la craníectomía. Por punción transcutánea a través de ella se mide la presión del espacio subdural de 26 cm de H20 apoyando el diagnóstico de HEA. Se coloca drenaje subduroperitoneal bilateral logrando una evolución favorable.
Conclusión. El manejo terapéutico óptimo de las colecciones subdurales aún no ha sido establecido. La conducta conservadora resulta adecuada en casos asintomáticos y sin efecto de masa mientras que en efusiones subdurates bastaría irrigar la cavidad o una derivación subduroperitoneal. Las derivaciones de LCR resultan de impredecible eficacia en HEA y las colecciones asociadas persisten o recidivan tras su evacuación, por lo que una correcta selección de pacientes es clave antes de cualquier decisión terapéutica.
Palabras clave: hematoma subdural, hidrocefalia externa, higroma subdural.
Correspondencia:
mrojas@fleni.org.ar
Recibido: junio 2011.
Aceptado: agosto 2011.
INTRODUCCIÓN
El término "higroma subdural crónico" fue acuñado por primera vez por Dandy en 1932 para designar una colección subdural no hemática encapsulada por fina membrana pudiendo resultar de un proceso cerebral atrófico, secuestro de líquido cefalorraquídeo (LCR) o hidrocefalia externa. Si bien ésta última ha sido descripta como un agrandamiento del espacio subaraenoideo o subdural, generalmente en contexto de hipertensión endocraneana (HTE) en población pediátrica, varios autores han postulado que la misma podría ocurrir también en adultos1.
A diferencia de la hidrocefalia común del adulto en la que los índices de cuernos frontales (FHI) y de Evans pueden aplicarse como medidas radiológicas, en el caso de la hidrocefalia externa del adulto (HEA) ambas resultarían inadecuadas al no poder reflejar el agrandamiento ventricular en el contexto de una colección. subdural'. Asimismo, los tratamientos basados en derivación o shunt de LCR resultan de impredecible eficacia en este cuadro, incluso pudiendo dar lugar a. resultados desfavorables, mientras que la simple evacuación de la colección subdural resulta inútil si la misma es una expresión radiológica de HEA, persistiendo o volviéndose a formar luego de su evacuación. Por todo esto, resulta de evidente importancia diferenciar un cuadro secundario a un hematoma subdural (HSD) crónico o higroma subdural de aquél, producto de una HEA antes de tomar decisiones terapéuticas.
PRESENTACION
Paciente de 73 años con antecedente de drenaje quirúrgico de HSD veintiún años atrás que presenta trastornos en la marcha y paresia braquial derecha de tres semanas de evolución por lo que consulta y es estudiado con tomografia computada (TAC) de cerebro constatándose un quiste aracnoideo temporal izquierdo previo, un HSD frontotemporoparietal izquierdo subagudo de 30 mm de espesor y desviación de línea media de 4 mm y un hematoma epidural (HED) frontotemporal asociado sin un relato claro de trauma craneoencefálico (TEC) reciente (Fig. 1). Se realiza evacuación quirúrgica del HSD y HED evolucionando en las primeras 12 hs del postoperatorio con deterioro del sensorio hasta llegar a GCS 7/15. En la TAC control se evidencia resangrado y nuevo HSD frontotemporoparietal izquierdo de 35 mm de espesor con desviación de línea media de 6 mm por lo que es intervenido nuevamente para drenaje quirúrgico del mismo y craniectomía descompresiva. Aún así, persiste con deterioro de su estado de conciencia y requerimiento de asistencia respiratoria mecánica (ARM) presentando las siguientes complicaciones durante su postoperatorio mediato: neumonía por Enterobacter asociada a respirador y shock séptico secundario a foco respiratorio con requerimiento de tratamiento antibiótico (ATB) endovenoso, neumotórax derecho con requerimiento de avenamiento pleural quirúrgico, status epiléptico tratado con carga de fenitoína y posterior rotación a levetiracetam por hepatotoxicidad, necesidad de traqueostomía por ARM prolongada a los 18 días de Iniciada la misma.
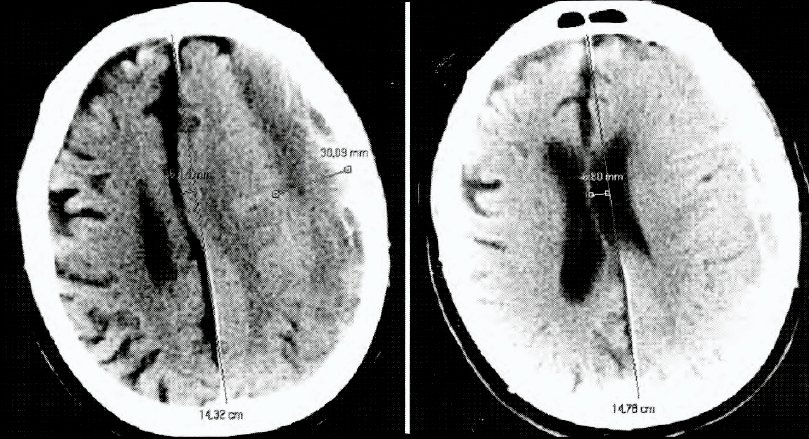
Fig. 1. TAC de cerebro. HSDfrontotemporoparietal izquierdo subagudo de 30 mm de espesor con desplazamiento de línea media.
Posteriormente, el paciente evoluciona con sensorio fluctuante, apertura ocular espontánea, confuso, con lenguaje disártrico e hipofluente, obedecimiento parcial de órdenes simples y sin déficit motor. En las TAC dev control se evidencian colecciones líquidas bilaterales extraaxiales con ventrículos no dilatados y surcos y cisternas levemente ensanchados pero conservados (Fig. 2 A). La craniectomía se presenta tensa con herniación de la colección a través de la misma por lo que se sospecha una posible hidrocefalia externa dados los antecedentes quirúrgicos múltiples y probable TEC que podrían implicar desgarro aracnoideo (Fig. 2 B). Se realiza TAC cerebro con contraste que pone en evidencia imágenes de venas corticales superficiales extendiéndose a través de las colecciones líquidas resultando compatible con el "signo de venas corticales" descripto para HEA (Fig. 3). El índice de cuernos frontales ventriculares modificado (m FHI) alcanza un valor del 30%, y si bien aquellos mayores a 35% se correlacionarían con cuadros de HEA, el valor hallado no resulta válido teniendo en cuenta el secuestro de líquido a través de la craniectomía. Finalmente se decide aprovechar el defecto craneano para realizar una punción transcutánea a través de la misma logrando medir la presión en el espacio subdural / subaracnoideo al conectar la aguja a un transductor de presión que resulta de 26 cm de H20, apoyando el diagnóstico de HEA en la que se toma como
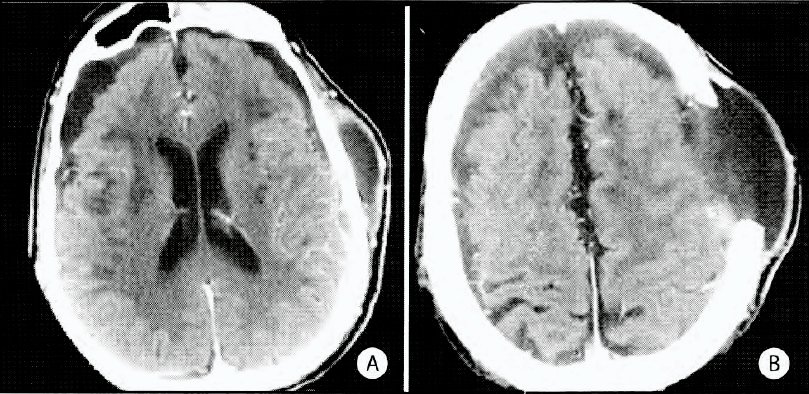
Fig. 2. TAC de cerebro: A. Colecciones extraaxiales bilaterales con ventrículos no dilatados y sin efecto de masa sobre corteza. B. Colección extraaxial con herniación a través de craniectomía.
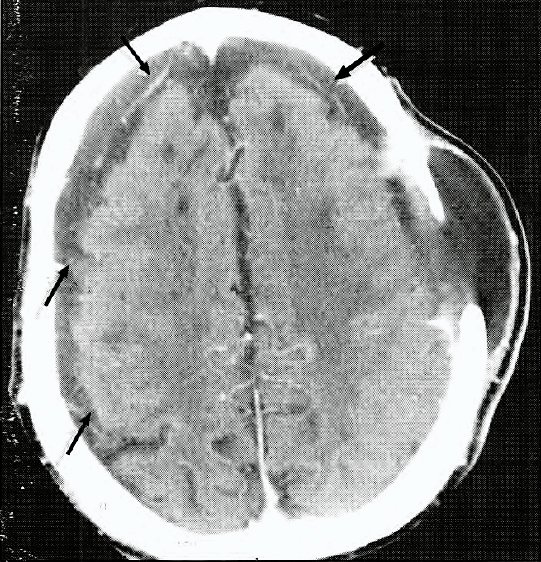
Fig. 3. TAC de cerebro con contraste. Venas corticales (flechas) extendiéndose a través de colecciones extraxiales ("signo de vena cortical").
Asimismo, el análisis fisicoquímico de una muestra evacuada de 60 ml del líquido revela: aspecto xantocrómico, ausencia de células, glucosa 108 mg/ dl, proteínas 230 mg/di, ácido láctico 5.6 compatible con LCR con modificaciones postquirúrgicas o líquido de efusión subdural secuelar. Los cultivos de la muestra resultan negativos.
A pesar de la posibilidad de tratarse de efusiones subdurales que suelen estar aisladas de la circulación de LCR por neomembranas vascularizadas, el comportamiento de la colección a través de la craniectomía así como la presión subdural medida y los hallazgos imagenológicos conducen al diagnóstico de HEA decidiéndose la colocación quirúrgica de un drenaje subduroperitoneal bilateral de catéteres frontales y conector en "Y" con válvula programable (a un valor de resistencia inicial de 100 mm de H20) que compensaría el déficit absortivo de LCR supuesto en estos casos pero con una resistencia al drenaje que evitaría la exacerbación de un cuadro de hidrocefalia externa y alejaría el riesgo de nuevos HSD por sobredrenaje de un shunt intraventri - cular. El paciente evoluciona de forma favorable con mejoría progresiva de su sensorio y cuadro de confusión e imágenes controles con resolución de HEA por lo que es dado de alta al día decimotercero postoperatorio (Fig. 4). Continúa asimismo con mejoría de su estado cognitivo constatado en controles ambulatorios periódicos que alcanzan hasta el primer año postoperatorio.
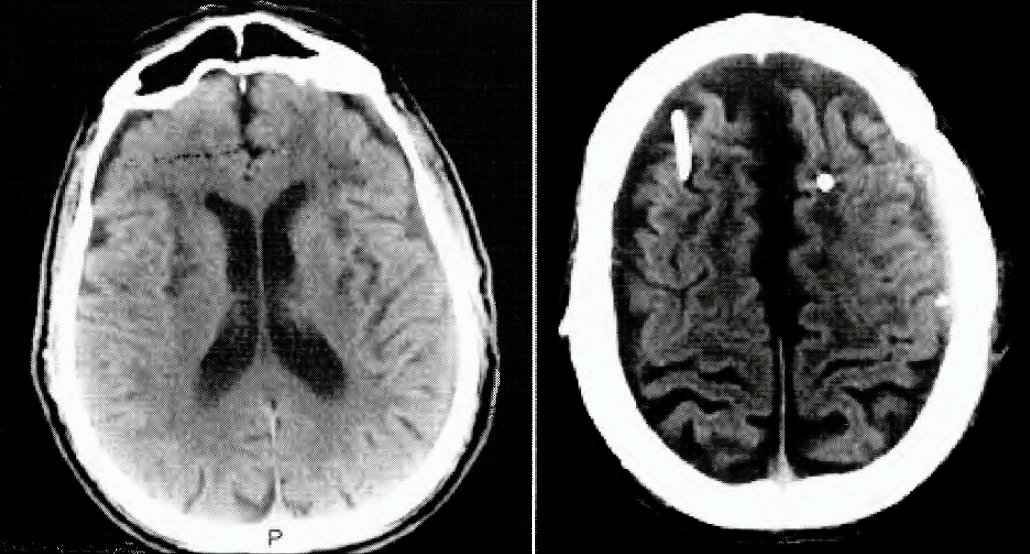
Fig. 4. TAC de cerebro. Control postoperatorio de shunt subduroperitoneal y craneoplastía que evidencia resolución de HEA.
DISCUSIÓN
El espacio subdural es un espacio virtual entre la capa interna dural y la aracnoides atravesado cerca de la convexidad por las venas puentes que conducen el drenaje venoso cerebral al seno longitudinal superior2. El concepto de "colección subdural" es un término radiológico utilizado para describir exceso de líquido en el espacio subdural que puede ser producto de diferentes causas, incluyendo procedimientos quirúrgicos previos, TEC, infecciones, malformaciones congénitas y craneocefálicas1. El mecanismo fisiopatológico para su formación aún no está aclarado completamente aunque se postula que habría una falta de cohesión entre duramadre y aracnoides consecuencia de un déficit de tejido colágeno u otras alteraciones a nivel de unión intercelular que junto, o no, a las causas predisponentes previamente mencionadas (trauma, infección, etc.) daría lugar a la transformación de un espacio subdural virtual en uno real en el que las membranas desgarradas aracnoidales funcionarían con un mecanismo valvular que impediría la restauración de la unión entre ambas meninges. Una hipótesis aceptada para explicar la acumulación de LCR subdural sería su salida a través de una pequeña rotura de la membrana subaracnoidea en presencia o no de sangre causada por microtraumas en las venas puentes que en su conjunto constituirían el denominado higroma subdural, que puede estar perpetuado por el efecto valvular aracnoideo mencionado. La presencia de un proceso infeccioso en el espacio subdural, como en el caso de la meningitis por Haemophilus Influenzae, constituye una causa menos frecuente de colección líquida subdural. Otras situaciones predisponentes para su aparición son las acumulaciones exvacuo secundarias a infartos cerebrales o a encefalopatía anóxica. Las colecciones subdurales representan del 7 al 12% de las masas intracraneales postraumáticas y. por lo general, pueden tardar hasta un mes en desarrollarse, período en el cual pueden presentarse manifestaciones clínicas inespecíficas (14 al 50% de los casos) desde las primeras 24 horas, siendo más frecuentes durante la primera semana. Comúnmente suelen cursar de forma asintomática y reabsorberse espontáneamente aunque, en ocasiones, pueden generar crisis, déficit focal o ejercer un notable efecto de masa, situaciones en las que resulta importante conocer su naturaleza para planificar su tratamiento1,2,3.
Como se mencionó. la aparición de colecciones líquidas subdurales puede deberse a mecanismos variables, entre los que se proponen:
- Desgarro aracnoideo con efecto valvular unidireccional de LCR: teoría fundamentada en estudios de Hoff et al quienes en 1973 evidencian en el espacio subdural de tres pacientes con higromas postraumáticos la presencia mediante cisternografía de Tc 99m inyectado por punción en el espacio subaracnoideo lumbar. Tanaka et al concluirían posteriormente que aunque los ancianos presenten con mayor frecuencia colecciones subdurales postoperatorias (probablemente relacionado con mayor grado de atrofia y menor capacidad de reexpansión cerebral) es en los pacientes jóvenes en los que las colecciones resultan mas frecuentemente sintomáticas, especialmente en aquellos con antecedentes de múltiples craneotomias. Según algunos autores, la disminución de la eiastancia cerebral y resistencia al flujo de salidas del LCR generadas por las craniectomías, especialmente las descompresivas, favoreceria la posterior formación de colecciones subdurales. Esto podría haber sucedido con nuestro paciente.
- Efusión subdural y formación de neomembranas vascularizadas: Stone et al encontraron mayor contenido proteico del líquido de higroma subdural postraumático en relación al LCR por lo que lo consideraron una efusión al espacio subdural desde capilares dañados del parénquima subyacente. Posteriormente, el análisis microscópico de meninges resecadas en pacientes con higromas postraumáticos revelarla la presencia de una neomembrana vascularizada con numerosas fenestraciones y pinocitosis bajo la duramadre. La efusión subdural podría ser un precursor del HSD crónico debido al sangrado repetido por la hiperfibrinólisis que tiene lugar en la membrana externa.
-Aumento de permeabilidad aracnoidea al pasaje de LCR: Licata et al en su serie de 4.000 pacientes con trauma craneal grave encontraron que 98 desarrollaron hidrocefalia postraumática, de los cuales en un tercio fue precedida por una colección transitoria subdural de LCR que se reducía progresivamente hasta desaparecer en relación inversa a la progresión de la hidrocefalia y que los autores adjudicaron a un aumento de permeabilidad en la uniones intercelulares aracnoideas o secundario a un gradiente de presión aumentado entre el espacio subaracnoideo y el subdural.
De esta manera, las colecciones subdurales según sus mecanismos etiopatogénicos podrían considerarse como efusiones cuando son de líquido xantocrómico hiperproteico encapsuladas por una neomembrana que realza con contraste en resonancia magnética (IRM) sin comunicación con el espacio subaracnoideo y relacionadas a un trauma craneal con daño vascular y/ o parenquimatoso asociado, mientras que los higromas serían acúmulos de LCR subdurales en comunicación libre con el espacio subaracnoideo a partir de un desgarro o tear aracnoideo frecuentemente secundario a un antecedente quirúrgico (especialmente de aneurismas intracraneanos)2.
La "hidrocefalia externa" es una entidad clínica bien definida en pediatría, caracterizada por macrocefalia, una evolución benigna autolimitada y colecciones extraaxiales hipodensas en TAC1,2,4, especialmente a nivel de las convexidades frontales, junto con preservación de los surcos corticales4, ensanchamiento de espacios subaracnoideos, cisternas basales nsura interhemisférica anterior con o sin leve agrandamiento ventricular4,5. Clínicamente pueden existir o no síntomas de HTE y no siempre se detecta una presión intracraneal aumentada3. Generalmente esta condición es reconocida durante ei primer año de vida y suele resolver espontaneamente hacia el segundo año3,5. Sin embargo, en un pequeño numero de pacientes la hidrocefalia externa puede evolucionar a una hidrocefalia comunicante interna progresiva sintomática requiriendo la implantación de un shunt de LCR luego de los dos años de edad3,4. Se ha postulado una alteración en la reabsorción de LCR como causa asociada a la conversión de hidrocefalia externa en interna, ademas de una inmadurez de la bóveda craneal y del parénquima cerebral, aunque se desconocen los verdaderos factores responsables1,3,4
Si bien la mayoría de los casos pediatricos son idiopáticos, algunos se asocian a macrocefalia congénita, varios tipos de craneostosis (especialmente plagiocefalia), traumas, infecciones o hipertensión venosa1,4. Los infantes resultan más propensos a las colecciones extraaxiales dada la falta de fusión final de las suturas craneanas, la plasticidad de un cráneo con osificación inmadura (con la consecuente macrocefalia secundaria) y la elasticidad de un tejido encefálico aún no mielinizado1 . Cuando el espacio subaracnoideo se agranda, la IRM o TAC con contraste pueden mostrar a las venas corticales superficiales extendiéndose a través de la colección líquida conformando el llamado "signo de la vena cortical", que permite diferenciar el ensanchamiento del espacio subaracnoideo de una colección hipodensa líquida subdural en la que el signo resultará. negativo dado que la compresión del espacio subaracnoideo por la colección aproxima las venas corticales a la superficie cerebral. Esta distinción radiológica entre colección subdural (generalmente traumática) y aracnoidea (o hidrocefalia externa) puede resultar de gran importancia, especialmente legal, en casos de posible abuso infantil5. La cisternografia nuclear ha resultado no concluyente en la evaluación de hidrocefalia comunicante en infantes y se ha reportado como normal en casos de niños con hidrocefalia externa4.
Todavía no hay consenso unánime sobre si la ubicación exacta de la colección extraaxial es de hecho a nivel del espacio subaracnoideo, por lo que el término de "hidrocefalia externa" no es universalmente aceptado. Algunos autores creen que el exceso de líquido toma lugar en el espacio subdural y prefieren hablar de "colecciones subdurales benignas". Otros evitan la controversia sobre la localización y apelan al término de "colecciones extraaxiales o extracerebrales benignas". Finalmente, también hay quienes evitan la polémica mediante un consenso global hipotetizando que el exceso de LCR puede acumularse en diferentes compartimentos intracraneanos y así se puede hablar de "hidrocefalia externa" cuando la acumulación líquida es a nivel extraaxial, "hipertensión intracraneana benigna" a nivel del intersticio cerebral o "hidrocefalia interna". cuando es a nivel intraventricular. Independientemente de si el líquido se acumula en el espacio subdural o subaracnoideo, todos los investigadores ,concuerdan en la existencia de una disfunción hidrodinámica en la interacción entre los volúmenes líquidos y la masa cerebral en la cavidad craneal4.
Las colecciones extraaxiales progresivas pueden ser vistas en pacientes adultos con higromas subdurales como en aquéllos con HEA, término prestado de la literatura pediátrica para describir cuadros en pacientes adultos que cursan con colecciones extraaxiales de baja densidad y ensanchamiento ventricular que pueden no siempre resultar de curso transitorio y benigno4. En este contexto, resulta útil para la demostración de agrandamiento ventricular en pacientes adultos con colecciones líquidas subdurales el uso del índice de cuernos frontales modificado (m FHI) que, en vez de ipelar a la distancia entre tablas internas como en el modo convencional, utiliza como parámetro a la distancia bicortical correspondiente al corte de mayor ancho para los cuernos frontales1.
Mientras los sintomas derivados de compresión encefálica por agrandamiento ventricular como trastornos en la marcha, incontinencia urinaria y déficits mnésicos son típicos de la hidrocefalia interna normopresiva del adulto, cuadros de confusión, cefaleas y trastornos de memoria suelen ser más característicos de la HEA. Tanto la sintomatología como el agrandamiento ventricular pueden establecerse de una forma más evidente desde una semana hasta dos meses posteriores a la evacuación de las colecciones subdurales en los casos en los que este procedimiento quirúrgico se impone como terapéutica inicial1, tal como ocurriera con nuestro paciente.
La HEA es una complicación conocida en el manejo quirúrgico de la hemorragia subaracnoidea (HSA) aneurismática en la que se la cree secundaria a un descenso en la absorción de LCR por parte de las vellosidades aracnoidales hacia los senos durales venosos y desgarro quirúrgico de la aracnoides que actuaría como mecanismo valvular unidireccional llevando a la acumulación subdural de LCR. Si bien los desgarros aracnoideos pueden atribuirse a los mismos episodios de HSA, principalmente se deben a la ruptura de grandes porciones de las cisternas basales, como la prequiasmática, de Liliequist o directamente de la lámina terminal hacia el espacie) subaranoideo que resulta de fundamental importancia para el neurocirujano, ya que con ella logra una depleción de LCR y mejor retracción del parénquima cerebral para acceder a los vasos intracraneales. A medida que la hidrocefalia progresa la fina membrana aracnoidal que limita la colección subdural es sometida a mayor presión y, si es vencida su capacidad de resistencia, su ruptura permite la liberación del LCR contenido al espacio subaracnoideo, desde el cual es redistribuido a los espacios de menor resistencia y mayor compliance, es decir, los ventrículos laterales (dada su menor superficie y mayor elasticidad de sustancia blanca periventricular en comparación con el área y sustancia gris corucal), tornándose el cuadro tras varias semanas en una hidrocefalia interna, lo cual puede ocurrir espontáneamente o posterior al drenaje quirúrgico de la colecciones6. Se han informado colecciones subdurales hasta en el 38% de los pacientes con HSA y en el 14,5% de los sometidos a cirugía de aneurisma sin HSA. El tiempo de aparición de la HEA es aproximadamente 26 días después del procedimiento quirúrgico del aneurisma y hasta en un 81% de los casos conllevan dilatación ventricular asociada7. De esta forma, en los orígenes de la HEA habría un exceso de LCR, producto de un desbalance entre su producción y absorción. que tendería a moverse libremente entre el compartimento subdural, subaracnoideo e intraventricular siguiendo los pasajes de menor resistencia determinados por la compliance intrínseca de cada estructura intracraneal. Una alteración absortiva de LCR explicaría también los fracasos de la tercerventrículostomía endoscópica reportados en casos de HEA6,7.
A pesar de las muchas similitudes radiológicas existentes entre los casos de atrofia cerebral, HEA e higromas subdurales, las tres resultan entidades clínicas distintas. Como describe Yoshimoto et al, la HEA suele presentarse en pacientes relativamente jóvenes y con evidencia de agrandamiento ventricular lateral mientras los higromas subdurales y la atrofia cerebral son más típicos de la población añosa1. Cardoso y Schubert han sugerido que las colecciones extraaxiales postraumáticas o posteriores a HSA referidas como higromas subdurales representarían en los añosos formas de HEA que deberían ser monitoreadas por imagen periódicamente, pues podrían evolucionar a hidrocefalia interna con el consiguiente requerimiento de una derivación de LCR. En esta instancia, resulta fundamental poder diferenciar entre HEA e higromas subdurales dado que mientras la primera resuelve generalmente tras la colocación de un shunt de LCR, los segundos suelen agrandar su tamaño como respuesta a la disminución del tamaño ventricular y volverse crónicos1,4. La IRM resulta superior a la TAC en la evaluación de la HEA ya que su intensidad de señal puede proveer información adicional sobre la composición líquida de la colección4. En la secuencia potenciada de IRM en T1 es posible distinguir la colección subdural de la subaracnoidea, esta última siendo isointensa con el LCR intraventricular, mientras que en la secuencia potenciada en T2, al igual que con la TAC con contraste, puede apreciarse la presencia de venas corticales en un espacio subaracnoideo ensanchado, conformando el mencionado "signo de la vena cortical"3. En la diferenciación de la HEA de otras colecciones subdurales, como higromas y HSD crónicos, debe tenerse en cuenta que en la primera los pacientes pueden mostrar dilatación ventricular a pesar de la colección extraaxial con preservación de surcos corticales, lo que indica una fuga de líquido hacia la convexidad redirigida por sistema de presiones hacia los ventrículos donde aumentan su presión como fue explicado anteriormente, mientras que en el caso de los higromas y/ o hematomas, estos desplazan la línea media y comprimen los ventrículos y espacios subaracnoideos ipsilaterales a su colección7. Todos estos parámetros imagenológicos alertan sobre una posible hidrocefalia.
Teniendo en cuenta que muchos autores han propuesto que la hidrocefalia postraumática resulta no sólo en agrandamiento ventricular sino también en HTE, la medición de presión en el espacio subdural/ subaracnoideo al hacer el orificio de trépano resulta un método diagnóstico válido para diferenciar cuadros de HEA, generalmente con presión superior a 15 cm de H20, de aquellos debidos a higromas subdurales simples1. Siguiendo este principio, se decidió en nuestro paciente la medición de presión del espacio subdural / subaracnoideo a través de una punción transcutánea conectada a transductor de presión aprovechando el defecto craneano de la craniectomía descompresiva.
El tratamiento de formas atípicas de hidrocefalia plantea problemas a la hora de decidir la conveniencia de realizar un procedimiento quirúrgico para la colocación de un sistema de derivación o shunt. La mala selección de pacientes puede llevar a fracasos terapéuticos y complicaciones fatales. En los casos de HEA posterior a HSA, dada su fisiopatología de fuga de LCR hacia la convexidad como la disminución en su absorción, la hidrocefalia no desaparecería con el simple drenado de la colección o la colocación de una derivación subduroperitoneal que potenciaría la fuga perpetuando e incrementando el riesgo de progresión clínica y efecto de masa del cuadro. Por otro lado, si bien está reportada la resolución espontánea de las colecciones asociadas en aproximadamente un 66% de los casos, también existe la necesidad de una derivación de LCR definitiva, como un shunt ventriculoperitoneal, en cerca del 30% en el que se reportan excelentes respuestas evitando un deterioro intelectual irreversible en los pacientes7.
Como se puede apreciar a partir de lo ya expuesto, la mayoría de las teorías que intentan explicar la HEA implican tres factores fundamentales: alguna forma de sangrado intracraneal, un desgarro aracnoideo y un acumulo de LCR secundario a un descenso en su absorción. Una alteración en la absorción de LCR produciría una acumulación del mismo proximal con aumento de la presión intraventricular superando la del espacio subaracnoideo y venas intraparenquimatosas según la ley de equilibrio de presiones intracraneales de Hakim. Sin embargo, este razonamiento no se aplicaría a los casos de HEA en los que se observan cisternas basales, surcos ipsilaterales a la acumulación subaracnoidea y ausencia de desplazamientos de línea media con o sin una ligera dilatación ventricular que dan cuenta de la igualdad de presiones a ambos lados del parénquima cerebral. Un punto importante en esta cuestión podría ser el hecho de que el espacio subaracnoideo es el primer compartimento de LCR que se dilata en respuesta a la fase inicial de la hidrocefalia, reduciendo la presión intracraneana y reestableciendo el equilibrio. Cuando este equilibrio no se alcanza, el aumento de presión haría que el LCR busque otra salida redirigiéndose a los ventrículos causando su dilatación. Que se alcance o no este equilibrio podría depender a su vez del grado de alteración en la absorción de LCR y de que el defecto aracnoideo presente efecto valvular o no, lo que determinará la variación en el tiempo del volumen de las colecciones. Así pues, en algunos estas desaparecerán totalmente en forma espontánea, en otros persistirá únicamente la colección extraaxial y en otros, finalmente, desaparecerá la acumulación en la convexidad para producirse una hidrocefalia clásica o interna. De esta forma, se podrían distinguir distintos tipos de pacientes:
- Los que mejoran espontáneamente después de un trauma, HSD agudo o cirugía y no desarrollan hidrocefalia en controles imagenológicos, que son la mayoría.
- Los que presentan colecciones extraaxiales con componente subaracnoideo en IRM, a veces con cierta dilatación ventricular pero con cisternas basales y surcos ipsilaterales a la colección conservados y sin desplazamiento de línea media. Estos pacientes pueden mejorar o no espontáneamente y deben ser controlados de cerca radiológicamente ya que pueden desarrollar una hidrocefalia interna que obliga a la colocación de una derivación ventricular de LCR, con posterior desaparición de la acumulación extraaxial. - Los que inicialmente se presentan de la forma anterior y evolucionan clínicamente de forma favorable espontáneamente pero con persistencia de la colección extraaxial. En estos casos no está indicada la derivación intraventricular y se plantea la colocación de una derivación subdural o simplemente el drenaje y lavado del mismo3.
A pesar de todo lo expuesto, el manejo terapéutico óptimo de las colecciones subdurales no ha sido establecido. Es un hecho, sobre el que insisten Lee el al, entre otros autores, que un higroma subdural tiene dos caminos posibles a seguir: se resuelve espontáneamente o evoluciona a un HSD crónico. La conducta conservadora se presenta como la más adecuada en casos asintomáticos y sin efecto de masa mientras que cuando se trata de efusiones subdurales podría bastar con irrigar la cavidad o colocar una derivación subduroperitoneal. De esta manera, resulta clave la selección de pacientes basada en la diferenciación correcta entre los que presentan HEA de los que presentan colecciones subdurales simples postraumáticas, ya que un shunt de LCR sería el tratamiento de elección para la primera mientras que exacerbaría las últimas. Si bien la derivación ventriculoperitoneal es la propuesta como apropiada para casos de colecciones asociadas a HEA, algunos autores prefieren de inicio la derivación subduroperitoneal ante toda colección subdural puesto que la primera podría aumentar aquellas colecciones en las que hay un componente de daño vascular o parenquimatoso asociado a trauma y formación de neomembranas vascularizadas, es decir las mencionadas "efusiones subdurales"1,2 .
Éste último fue el criterio que decidimos aplicar a nuestro paciente al implantarle una derivación subduroperitoneal bilateral, ya que si bien la colección extraaxial que presentaba en contexto de sutil dilatación ventricular se herniaba a través del defecto óseo craneal provocado por la craniectomía, por consiguiente, comportándose como una HEA, también resultaba cierto que dicha colección se había originado a partir de un HSD probablemente postraumático, considerando el HED asociado, por lo que conllevaba mayor componente de efusión que de higroma simple subdural (diferenciación apoyada también en los hallazgos fisicoquímicos del líquido evacuado) por lo que quisimos evitar el riesgo de que se agrandara posteriormente a la colocación de un shunt ventriculoperitoneal. Asimismo, la elección de una válvula programable en la derivación nos permitiría controlar el grado de drenaje de las colecciones en caso de que se exacerbaran tras el mismo ya que, si bien las efusiones se consideran aisladas de comunicación con el LCR por su neomembrana envolvente, las múltiples intervenciones quirúrgicas con evacuaciones de colecciones líquidas y aperturas de neomembranas con seguridad habrían implicado desgarros aracnoideos acompañantes. Afortunadamente la respuesta al tratamiento quirúrgico de derivación subduroperitoneal de LCR por parte del paciente así como su evolución posterior fueron favorables resolviendo tanto los hallazgos clínicos como imagenológicos causados por el cuadro.
Finalmente, se debe mencionar que muchos autores consideran útil la aplicación de un ciclo de corticoides durante dos semanas en la fase inicial de las colecciones postquirúrgicas fundamentando que esto disminuiría la producción de LCR así como la dificultad en su absorción previniendo una HEA incipiente2.
CONCLUSIÓN
La HEA se asocia a traumas, HSA y neurocirugías, especialmente las relacionadas con aneurismas, manifestándose como cuadros de confusión, cefaleas y trastornos de memoria. Se produce una expansión del espacio subaracnoideo /subdural y la mayoría de las teorías que intentan explicarla implican tres factores fundamentales: alguna forma de sangrado intracraneal, acúmulo de LCR secundario a un descenso en su absorción y un desgarro aracnoideo que actuaría como mecanismo valvular unidireccional llevando a la acumulación extraaxial de LCR. El manejo terapéutico óptimo de las colecciones subdurales aún no ha sido establecido adecuadamente. La conducta conservadora se presenta como la más adecuada en casos asintomáticos y sin efecto de masa mientras que cuando se trata de efusiones subdurales podría bastar con irrigar la cavidad o colocar una derivación subduroperitoneal. Los tratamientos basados en derivación o shunt de LCR resultan de impredecible eficacia en casos de HEA, incluso pudiendo dar lugar a resultados desfavorables, mientras que la simple evacuación de la colección extraaxial asociada resulta inútil, persistiendo o volviéndose a formar luego de su drenado. Por todo esto, resulta clave previo a la toma de decisiones terapéuticas una adecuada selección de pacientes basada en la diferenciación correcta entre aquellos que presentan HEA de los que presentan colecciones subdurales simples postraumáticas, ya que un shunt de LCR sería el tratamiento de elección para la primera mientras que exacerbaría las últimas. La signosintomatología del paciente, sus antecedentes, la IRM, con ventaja sobre la TAC, el FHI, la medición de presión del espacio subdural/subaracnoideo y el análisis fisicoquímico del líquido de la colección extraaxial resultan orientadores en la discriminación de los distintos cuadros.
Bibliografía
- Huh PW, Yoo DS, Cho KS, Park CK, Kang SG, Kim DS et al. Diagnostic method for differentiating external hydrocephalus from simple subdural hygroma. J Neurosurg 2006; 105: 65-70.
- Miranda P, Lobato RD, Rivas JJ, Alén JF, Lagares A. Colecciones subdurales postraumáticas: presentación de un caso y revisión de la literatura". Neurocirugía 2003; 14: 67-71.
- Escosa-Bagé M, Sola RG. Fisiopatología de la hidrocefalia externa del adulto". Rey Neurol 2002; 35(2): 141-4.
- Cardoso É. Schubert R. External hydrocephalus in adults. J Neurosurg 1996; 85:1143-7.
- Kuzma B, Goodman J. Differentiating external hydrocephalus from chronic subdural hematoma. Surg Neurol 1998; 50: 86-8.
- Rahme R, Bojanowski MW. Infernal hydrocephalus, external hydrocephalus, and the syndrome of intracerebral cerebrospinal fluid entrapment: a Challenge to current theories on the pathophysiology of communicating hydrocephalus. Medical IIypotheses 2010; 74: 95-8.
- Arriada-Mendicoa N, Herrera-Guerrero MP, Otero SE. Hidrocefalia crónica del adulto. Reto diagnóstico y terapéutico. Rey Neurol 2002; 34(7): 665-72.
ABSTRACT
Objective. Report of an externa! hydrocephalus (HE) case in an adult patient.
Material and method. 73 year old patient with gait disorders and right brachial paresis of three weeks of evolution secondary to a subdural hematoma located in the leftfrontotemporoparietal area.
Intervention. After performing a dual drainage and decompression craniectomy due to rebleeding in the immediate postoperatory period, the patient evolved with ajluctuating sensory system and confusion. Thefollow up CT scans showed bilateral extra-axialfluid collections with preserved ventricles, sulci and cisterns, the "cortical vein sign" through every collection and herniation into the craniectomy site. The transcutaneous puncture measured a pressure of 26cm of H20 in the subdural space thus supporting the diagnosis of EH. A bilateral subduroperitoneal shunt was placed achieving afavorable result.
Conclusion. The optima( therapeutic management of subdurai collections has not been well established yet. A conservative approach is aaeguate in asymptomatic cases without mass effect whilst in subdural effusions it would suffice to irrigate the cavity and/ or place a subduroperitoneat shunt. CSF diversions have an unpreciictable efficacu in EH and the associatea collecttons persist or recur qfter being drained. Therefore. corred t batiera selection is critica! bejore anu therapeutic aecision is macie
Key words: subdural hematoma, external hydrocephalus, subdural hygroma.
COMENTARIO
Los autores presentan un interesante y controversial caso de hidrocefalia externa del adulto (HEA) en el contexto de un hematoma subdural crónico o viceversa. En una exhaustiva y prolija revisión bibliográfica, tratan de dilucidar y establecer la fisiopatologia y el diagnóstico dlierencial entre las distintas colecciones extracerebrales, de las que no hay consenso en la literatura.
Los autores insisten en la necesidad de diferenciar ambas patologías: la HEA de las colecciones subdurales (hematoma subdural crónico, higroma subdural), y lo enfatizan al decir que ".., los tratamientos de derivación del LCR resultan de impredecible eficacia en este cuadro, incluso pudiendo dar lugar a resultados desfavorables, mientras que la simple evacuación de la colección subdural resulta inútil si la misma es una expresión radiológica de HEA, persistiendo o volviéndose a formar luego de su evacuación" (pág. 1)
Analizando los antecedentes del paciente, tal vez a los autores les haya pasado inadvertido el hecho de que el paciente presentaba un quiste aracnoideo temporal izquierdo, homolateral al hematoma subdural frontotemporal agudo "sin un relato claro de trauma" y que obligó a la evacuación quirúrgica. El paciente refiere un antecedente de haber sido operado 21 años atrás, también de hematoma subdural.
Probablemente en ambas circunstancias la causa del hematoma subdural fueron desgarros espontáneos o por mínimos traumas de la vascularizada pared del quiste aracnoideo que permitió el pasaje de LCR con algo de sangre al espacio subdural con la consiguiente colección en dicho espacio. Es por eso que, a diferencia de otras escuelas, nosotros indicamos cirugía en los quistes aracnoideos Galassi II y III, aunque sean asintomáticos en los niños, para evitar situaciones futuras de emergencia neuroquirúrgica.
Ante la desfavorable evolución del paciente, los autores, con buen criterio, sospecharon la presencia de HEA subyacente al hematoma subdural, que se reafirmó con el signo imaginológico "signo de las venas corticales", patognomónico para diferenciar HEA del hematoma subdural crónico. Para confirmar su diagnóstico efectuaron una punción transcutánea que arrojó 26 cm H2O, valor que si bien puede ser discutible su exactitud por la acción de la presión atmosférica sobre la craniectomía, demostró hipertensión endocraneana. La derivación subduroperitoneal y/o subaracnoideo peritoneal mejoró definitivamente al paciente.
La crítica que puede hacerse al tratamiento es que faltó un adecuado estudio de la dinámica del flujo de LCR y que no es necesaria la colocación de dos catéteres proximales con el conector en Y, dado que hay mayor número de conexiones, aumenta la probabilidad de disfunción del shunt. Tanto en la HEA como en las colecciones subdurales, en el 95% de los casos ambos hemisferios están comunicados. También aconsejarnos la pronta cranioplastia para evitar futuras disfunciones hidrodinámícas en este paciente.
Los autores hacen una excelente revisión bibliográfica que demuestra la controversia existente tanto en la definición como en la etiología y tratamiento de las distintas colecciones extracerebrales.
La hidrocefalia externa es una entidad poco frecuente en niños y menos frecuente aún en adultos. Tampoco se puede extrapolar al adulto la interpretación de la hidrocefalia externa del niño, donde la principa) causa es la inmadurez de las granulaciones de Paccioni, generándose una desproporción entre la producción y absorción de LCR, generalmente transitoria y que se resuelve espontáneamente con el cierre de las suturas alrededor de los 2 años de edad.
Con esta presentación y revisión de la literatura los autores han traído a nuestra conciencia la necesidad de pensar bien la conducta terapéutica a seguir cuando se nos presente un caso tan complejo como el que motivó este trabajo.
Graciela Zuccaro
